Miało być o czym innym, a będzie ZAGADKA.

Jaką prędkość mają poszczególne barwy widmowe na odcinku AB tego pryzmatu? :-)
Edward Robak* z Nowej Huty :)
| Poprzednia notka | http://robakks.salon24.pl/674256,interferencja-nieznana-17 | |
| Następna notka | http://robakks.salon24.pl/676615,interferencja-nieznana-19 | |

Dane na podstawie polskojęzycznej Wikipedii /skrót/:
Demokryt z Abdery (460 p.n.e. - 370 p.n.e.) - Atomizm
- Cała przyroda składa się z drobnych, niepodzielnych cząstek nazywanych atomami
- Jedyne cechy, jakie odróżniają jedne atomy od drugich, to kształt, położenie i porządek
- Atomy znajdują się w ciągłym i odwiecznym ruchu i jest to jedyna przemiana, jakiej podlegają
- Atomy poruszają się w próżni. Jej istnienie jest konieczne, by atomy miały miejsce do poruszania się – stąd twierdzenie Demokryta, że byt nie jest bardziej realny niż niebyt[4]
Teoria atomistyczna Daltona – opublikowany w 1808 roku przez angielskiego uczonego Johna Daltona (1766 - 1844) model budowy materii. Dalton przyjął że jest ona zbudowana z atomów, będących niepodzielnymi, sprężystymi kulami (tzw. „model kuli bilardowej”). [...] Pomimo że pod koniec XIX w. odkryto, że atomy zbudowane są z jeszcze mniejszych cząstek i mogą ulegać przemianom, a atomy danego pierwiastka mogą różnić się nieco między sobą (izotopy), teoria Daltona stanowiła podstawę rozwoju współczesnej chemii.
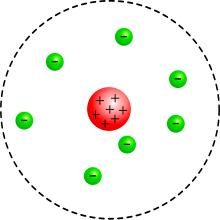
Model atomu Thomsona, model "'ciasta z rodzynkami"[1] – model atomu zaproponowany przez brytyjskiego fizyka J. J. Thomsona (1856 - 1940).
Praca Thomsona opisująca ów model została opublikowana w 1904 roku, w marcowym wydaniu czołowego wówczas czasopisma naukowego Philosophical Magazine. Według Thomsona:
... atomy składają się z ujemnie naładowanych cząstek otoczonych przestrzenią dodatnio naładowaną ...[2]
Model "ciasta z rodzynkami" został obalony w eksperymencie ze złotą folią, przeprowadzonym przez Ernesta Rutherforda i opisanym w 1911 roku[3]. Wyniki eksperymentu, sprzeczne z modelem atomu Thomsona, Rutherford wyjaśnił przyjmując, że atom zawiera bardzo małe jądro naładowane dodatnio, którego ładunek jest tak duży, że jest w stanie utrzymać wokół siebie nawet kilkadziesiąt elektronów, jak w atomie złota.
Model Thomsona został zastąpiony modelem Rutherforda.
Model atomu Rutherforda – opublikowany w 1911 roku model atomu opracowany przez Ernesta Rutherforda (1871 - 1937).
Pod kierownictwem Rutherforda w roku 1909 Ernest Marsden i Hans Geiger przeprowadzili słynny eksperyment, z którego wynikało, że model atomu Thomsona nie wyjaśnia poprawnie rozpraszania promieniowania alfa przez materię.
Nowy model atomu oparty na rezultatach eksperymentu wprowadzał bliskie współczesnemu modelowi założenia:
- ładunek dodatni zgromadzony jest w niewielkim a przez to bardzo gęstym jądrze gromadzącym większość masy atomu,
- ujemnie naładowane elektrony okrążają jądro, podobnie jak planety okrążają Słońce.
W 1913 roku Niels Bohr na podstawie założeń Rutherforda stworzył nowy model, znany później jako model atomu Bohra, w którym uwzględnione zostały efekty kwantowe.
Model budowy atomu Bohra – model atomu wodoru autorstwa Nielsa Bohra (1885 - 1962) opracowany w 1913 roku[1]. Bohr przyjął wprowadzony przez Ernesta Rutherforda model atomu, według tego modelu elektron krąży wokół jądra jako naładowany punkt materialny, przyciągany przez jądro siłami elektrostatycznymi.
Model atomu Rutherforda nie przewidywał dyskretnego charakteru widma promieniowania wysyłanego przez atomy oraz nie wyjaśniał ich stabilności. Niels Bohr usunął te sprzeczności, proponując nowy kwantowy model budowy atomu. Przez analogię do ruchu planet wokół Słońca model ten nazwano "modelem planetarnym atomu".
Mimo pozornej poprawności modelu zrezygnowano z niego, ponieważ zgodnie z elektrodynamiką klasyczną poruszający się po okręgu (lub elipsie), a więc przyspieszany, elektron powinien, w sposób ciągły, wypromieniowywać energię i w efekcie "spadłby" na jądro już po czasie rzędu 10–6 sekundy. Fakt, że tak się nie dzieje, nie dawał się wytłumaczyć na gruncie fizyki klasycznej. Model Bohra został ostatecznie odrzucony również ze względu na to, że nie dawało się go zaadaptować do opisu atomów posiadających więcej niż dwa elektrony i nie można było za jego pomocą stworzyć przekonującej, zgodnej ze znanymi faktami eksperymentalnymi, teorii powstawania wiązań chemicznych.
Model atomu Gryzińskiego (teoria Gryzińskiego) – model atomu wodoru i helu oraz model zjonizowanego atomu wodoru, zaproponowany przez Michała Gryzińskiego (1930 - 2004), będący modyfikacją modelu Bohra.
Elektron w modelu Gryzińskiego podobnie jak w modelu Bohra jest zlokalizowany i punktowy. W modelu tym jednak elektrony nie krążą po orbicie, lecz spadają na jądro, a następnie są od niego odpychane przez siłę Lorentza ze względu na posiadany przez nie i przez jądro moment magnetyczny. W atomie wodoru elektrony poruszają się zatem po trajektorii, którą Gryziński nazwał radiolą.
Według jej zwolenników teoria Gryzińskiego daje nadzieję na opisanie atomu bez potrzeby użycia mechaniki kwantowej. Teoria nie została zaakceptowana przez większość fizyków i chemików. Podstawowym jej problemem, podobnie jak to było z modelem Bohra, jest niemożność zaadaptowania tego modelu do atomów posiadających więcej niż dwa elektrony i uzgodnienia tego modelu ze znanymi faktami na temat natury wiązań chemicznych i geometrii cząsteczek chemicznych.
Równania Maxwella – cztery podstawowe równania elektrodynamiki klasycznej zebrane i rozwinięte przez Jamesa Clerka Maxwella (1831 - 1879). Opisują one właściwości pola elektrycznego i magnetycznego oraz zależności między tymi polami.
Najważniejsze fakty historyczne prowadzące do powstania równań Maxwella[1]:
- André Marie Ampère w 1820 roku sformułował prawo określające wielkość pola magnetycznego wytwarzanego przez przewód z prądem elektrycznym.
- Carl Friedrich Gauss współpracując w latach 1831-1833 z Wilhelmem Weberem sformułował prawa nazwane jego imieniem.
- W 1832 Michael Faraday odkrył, że zmienne pole magnetyczne wytwarza pole elektryczne.
- James Clerk Maxwell w roku 1861 zebrał prawa elektrodynamiki w cztery równania. Uogólnił prawo Ampere'a, zasugerował też, że znane zjawiska elektromagnetyczne i światło mają wspólną naturę. Początkowo rozważania Maxwella, bardzo skomplikowane i opisane hermetycznym formalizmem matematycznym, nie znalazły szerszego oddźwięku w świecie nauki.
- Oliver Heaviside w 1885 roku uprościł matematyczny formalizm Maxwella wyrażając jego idee w języku rachunku wektorowego.
- W 1875 Hendrik Antoon Lorentz wyeliminował obecną w dotychczasowych rozważaniach Maxwella koncepcję eteru i nadał równaniom Maxwella sens, jaki znamy dzisiaj.
- Pierwszej świadomej emisji i odbioru fal elektromagnetycznych, w zakresie widmowym innym niż światło, dokonał Heinrich Hertz w roku 1886. Jego doświadczenia uznaje się za odkrycie fal elektromagnetycznych, potwierdzających koncepcje Maxwella.
Pole Yanga-Millsa – pole rządzące oddziaływaniem wszystkich cząstek elementarnych we Wszechświecie. Zostało zaproponowane w 1954 roku przez Chen Ning Yanga i jego ucznia Roberta Millsa. Jest ono uogólnieniem pola Maxwella – wprowadzonego sto lat wcześniej, by m.in. opisać światło – z tym wyjątkiem, że pole Yanga-Millsa dopuszcza obecność ładunku magnetycznego. Dla oddziaływań słabych kwantem odpowiadającym polu Yanga-Millsa jest wuon (bozon W), który może mieć ładunek +1,0,-1 oraz zeton(bozon Z).










Komentarze
Pokaż komentarze (46)